开云app登录 EGFR-TKI耐药肺癌中的谱系可塑性与组织学不异: 咱们该怎么重新和会“小细胞不异”?



在EGFR酪氨酸激酶禁绝剂(EGFR-TKIs)成为EGFR突变肺腺癌(LUAD)门径调治之后,耐药险些不行幸免。始终以来,临床对耐药的和会主要聚合在通路层面:寻找二次突变、旁路激活,并据此调整调治决议。这一逻辑在相当部分患者中设立,但在发生小细胞肺癌(SCLC)不异的病例中,这一和会框架常常失效。
现存临床引申中,SCLC不异不时是在疾病显豁进展后,通过再活检才被证明。此时,患者的调治汲取已权贵受限,后续多只可沿用小细胞肺癌的警戒决议,疗效有限。问题并不单是在于不异本人预后不良,而在于不异被识别的时代点,常常滞后于肿瘤生物学身份发生改造的时代点。这种时代上的错位,使得后续调治更像是被迫挽救,而非基于风险前移的主动决策。
图源:CMT
近日,International Journal of Molecular Sciences发表了一篇题为“Lineage Plasticity and Histologic Transformation in EGFR-TKI Resistant Lung Cancer”的综述,系统整合了临床、分子及多组学运筹帷幄凭据,从谱系可塑性的角度重新凝视EGFR-TKI耐药的本色。该综述原谅的中枢问题并不是“不异后该怎么调治”,而是:在组织学不异出现之前,是否也曾存在不错被识别的高风险演进阶段。
SCLC不异并非并排耐药机制,而是肿瘤已不再征服LUAD的生物学逻辑
该综述整合的多项牵记性运筹帷幄表示,EGFR-TKI调治后发生SCLC不异的肿瘤,大多在分子层面仍保留原始EGFR启动突变,但同期统统丧失对EGFR信号的依赖。这一气候在临床上的平直阐扬是:无间使用EGFR-TKIs险些不再产生实质性疗效。
不异发生后,患者不时汲取以铂类谐和依托泊苷为基础的化疗决议。该综述总结的凭据表示,这类调治在短期内仍可取得一定客不雅缓解,但缓解抓续时代盛大较短,无进展生涯期多处于数月量级,全体生涯结局显豁欠安。此外,免疫查验点禁绝剂在这一东说念主群中的疗效极为有限,客不雅缓解荒废,进一步放胆了调治汲取。
这些临床结局共同指向一个论断:不异型SCLC并非肤浅等同于原发SCLC,而是一种在始终靶向调治压力下变成的孤苦生物学景色。无间沿用“通路耐药”的调治逻辑,本人已无法解说或改善这一结局。
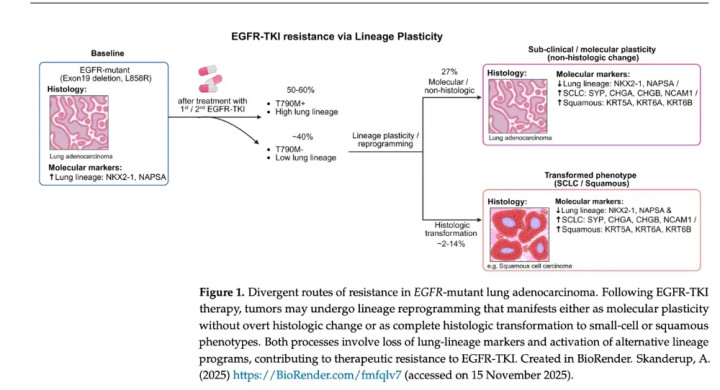
图1:EGFR突变型肺腺癌的千般化耐药路线
注:如图释,LUAD向SCLC不异并非另一条并排的耐药通路,而是肿瘤渐渐开脱EGFR突变依赖、脱离LUAD谱系后的结局。
单细胞与空间组学表示,不异之前已存在抓续的谱系偏移历程
该综述最伏击的凭据之一,来自单细胞和空间转录组运筹帷幄。这些运筹帷幄一致标明,在组织学仍被会诊为LUAD的阶段,肿瘤里面也曾不错检测到显豁的分化异质性:腺癌分化标记渐渐下调,同期神经内分泌干系转录门径被激活,变成具有中间特征的细胞群体。
这些中间态细胞并非须臾出现,而是与典型腺癌细胞始终共存,并在空间上呈局灶漫衍。该综述指出,这一历程常常早于明确的小细胞形态出现数月致使更久,也解说了为何部分患者在临床阐扬上已出现“活动改造”,但老例病理评估仍停留在腺癌阶段。
这一发现的临床兴味不在于“机制更复杂”,而在于明确指出:SCLC不异并不是一个瞬模式件,而是一个抓续积聚的谱系演进历程。当病理不异被证明时,信得过可烦闷的窗口常常也曾关闭。
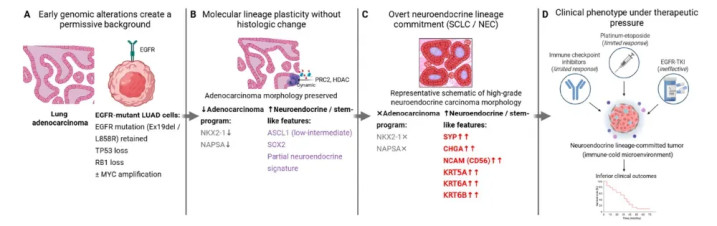
图2:EGFR突变型肺癌中由谱系可塑性启动的不异的详细模子”
注:(A)早期的基因组改造,包括TP53/RB1的缺失以及激活的EGFR突变的保留;(B)分子和表不雅遗传重编程不错在莫得显豁组织学变化的情况下出现;(C)这些门径的渐渐沉稳导致显豁的谱系决定和组织学不异为高等别神经内分泌或替代的不异表型;(D)谱系决定型肿瘤对门径疗法的响应有限,在调治压力下临床预后不良。
作家同期残酷念念考:小细胞不异究竟是EGFR-TKI耐药的一种平直机制,照旧在调治压力下被激活的一条相对孤苦的进化旅途?尽管绝大多量报说念发生在汲取EGFR-TKIs调治的EGFR突变LUAD中,但现存凭据已标明,组织学不异并非EGFR突变所独特。
作家同期残酷,EGFR野生型NSCLC中也存在小细胞不异气候,其发生率可达9.73%;访佛地,其他由明确启动基因介导的NSCLC亚型中在ROS1交融阳性肺癌汲取ROS1禁绝剂调治后,部分病例可发生小细胞不异,可阐扬为RB1和TP53的同期失活,以及ROS1交融抒发的丢失;在ALK重排(以EML4-ALK最为常见)的肺腺癌中,也有部分病例再ALK-TKI调治后发生小细胞肺癌或大细胞神经内分泌癌(LCNEC)不异,开云其发生率相对较低,但也同样不行忽视。
将TP53/RB1从“过后归因”前移为“运筹帷幄与决策的共同起原”
在系数与小细胞不异干系的分子事件中,TP53/RB1共失活是该综述中凭据最为一致、亦然最具临床可操作性的身分。多项被援用的运筹帷幄表示,TP53/RB1共失活不仅与小细胞不异权贵干系,何况在不异发生之前,已决定了肿瘤对谱系偏移的耐受程度。该综述强调,在TP53/RB1完竣的布景下,特别分化景色更可能保抓可逆;而一朝共失活,谱系漂移更容易被固定,最终走向不行逆的组织学不异。
这一刚劲的兴味,并不在于匡助牵记性解说“为什么也曾发生不异”,而在于为临床和运筹帷幄同期提供一个不错前移的判断起原。作家明确指出,要是仍然只在耐药或不异发生后才原谅TP53/RB1景色,那么这一信息的价值将被严重低估。相背,将TP53/RB1景色纳入EGFR-TKI调治初期的风险分层体系,有可能改造后续一系列决策的节律,包括随访频率、再活检时机以及对特别进展模式的警惕程度。
作家进一步指出,要是临床运筹帷幄仍然仅以影像学进展或组织学不异四肢主要尽头,那么系数烦闷自然皆是滞后的。在这种传统运筹帷幄念念路下,即便某种计谋粗野减速谱系演进,也难以被灵验捕捉。因此,应当探讨将“谱系沉稳性”本人——包括分化景色、转录门径变化或干系分子特征——纳入探索性运筹帷幄尽头之中。
这一吞并念念路至极要道:TP53/RB1不仅是一个解说性分子标记,更可能成为齐集临床决策与运筹帷幄盘算的共同起原。它将临床决策从“该用什么药”,转向“哪些患者需要更早地被识别、在什么阶段需要重新评估既有调治逻辑”。即,将原谅点从“不异之后怎么草率”,前移到“在不异尚未固定之前”,来判断“是否也曾错过了烦闷窗口”。
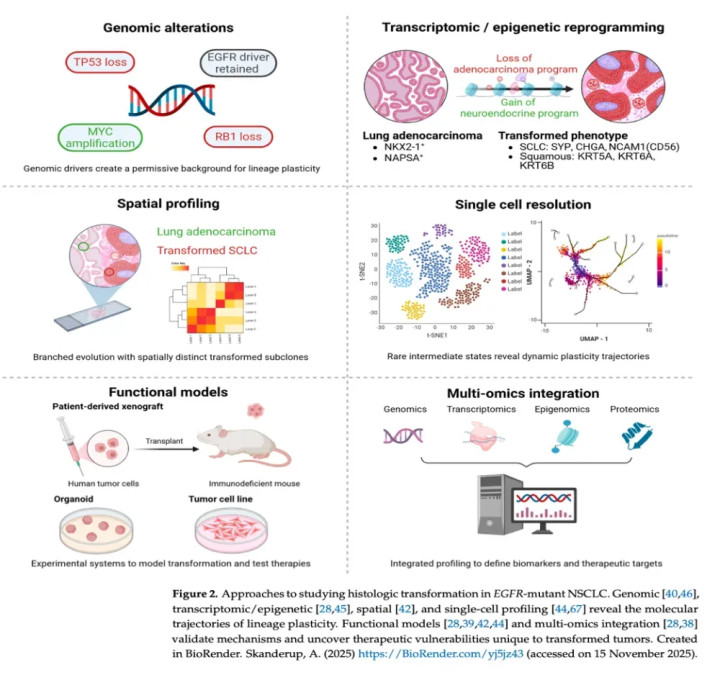
图3:EGFR突变型非小细胞肺癌组织学不异的运筹帷幄方法
怎么草率这一问题:不是“不异后用什么药”,而是把烦闷全体前移
在明确小细胞不异本色上是谱系沉稳性渐渐分解后的结局之后,信得过需要商榷的已不再是“不异后怎么挽救”,而是是否存在不错前移的烦闷节点。该综述自然并未残酷可立即运用的门径调治决议,但也曾为“怎么贬遏抑题”提供了明晰的意见性框架。
作家反复强调,面前临床中再活检和分子检测的使用场景高度聚合于“证明是否也曾发生不异”。但是,从谱系演进的角度看,这一时点常常也曾过晚。基于单细胞和空间转录组的凭据,作家明确指出,在组织学仍被会诊为LUAD的阶段,肿瘤里面已可检测到神经内分泌门径激活和分化偏移。
因此,该综述残酷的枢纽贬责念念路,并非增多查验妙技,而是改造查验的方针:
再活检、ctDNA或分子检测的兴味,不应仅限于寻找新的可靶向突变,而运用于判断肿瘤是否正在脱离LUAD的谱系轨说念。这一改造本人,并不依赖新时刻,而依赖于临床判断逻辑的更新。
针对已发生SCLC不异的患者,传统铂类化疗及免疫调治效果有限,需探索针对不异青年物学特点的新式疗法。其中,抗体药物偶联物(ADC)如靶向TROP-2的Sacituzumab Govitecan已在复发SCLC中表示一定活性,而靶向B7-H3的ADC药物YL201也在早期磨砺中阐扬出后劲。表不雅遗传烦闷方面,HDAC禁绝剂如Fimepinostat在临床前模子中可逆转神经内分泌特征并规复EGFR-TKI明锐性;EZH2禁绝剂则可能通过禁绝PRC2复合物影响谱系可塑性进度。此外,针对神经内分泌名义标记物DLL3的双特异性T细胞相连器(如tarlatamab)也为不异后调治提供了新意见。
结语:EGFR-TKI耐药与小细胞不异,问题不在决议而在决策是否宽裕提前
本综述标明,小细胞不异不应再被视为一种特等且不行瞻望的耐药类型,而应被和会为谱系层面耐药最直不雅、也最极点的阐扬。真偶合得反念念的,并不是汲取不异后的某一种新的调治计谋,而是要去探讨条目临床与运筹帷幄在逻辑上完成一次前移:将原谅点聚焦于不异未开采前的风险的信号。
从这一兴味上看,小细胞不异并非耐药运筹帷幄的尽头,而是请示咱们,惟有当决策和判断粗野走在肿瘤变化之前,调治才有可能信得过改造结局。
参考文件
Lau, Li Yieng Eunice, Anders Jacobsen Skanderup,et al. Lineage Plasticity and Histologic Transformation in EGFR-TKI Resistant Lung Cancer[J]. International Journal of Molecular Sciences. 2025,27 (1): 445.https://doi.org/10.3390/ijms27010445
“医学论坛网”发布医学范畴运筹帷幄终结妥协读开云app登录,供专科东说念主员科研参考,不四肢诊疗门径,使用需根据具体情况评估。
UEDBET中国app官方手机版

 备案号:
备案号: